各種耐性菌の話
メチシリン耐性黄色ブドウ球菌(MRSA)
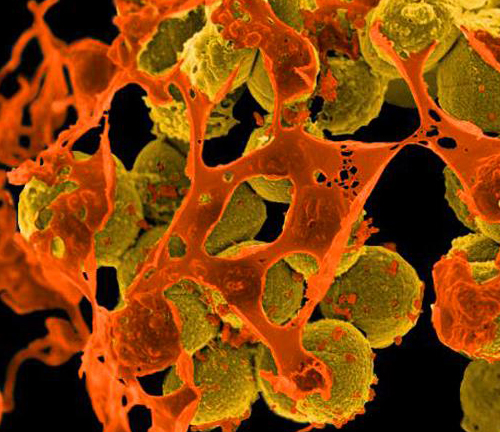
National Institute of Allergy and Infectious Diseases (NIAID).
黄色ブドウ球菌感染症、特にMRSA感染症は、治療が難しく気の抜けない、死亡率の高い感染症のひとつです。黄色ブドウ球菌は悪性腫瘍のように血流から各臓器に“播種する”傾向があり、しばしば治療に難渋します。黄色ブドウ球菌菌血症のマネジメントに感染症の専門家が入ることで患者予後が改善するという報告も複数あります[1]。MRSAは院内感染の原因菌として1970年代から問題となっていましたが、現在は市中にも広がっています。これらのMRSAは多少性格が異なることから「院内感染型MRSA」「市中感染型MRSA」と区分されることもあります。日本におけるMRSA分離率は減少傾向にありますが、市中感染型MRSA感染症は増えているといわれており[1]、院内感染コントロールだけでなく、市中のMRSAをどうコントロールするかも課題となります。
ペニシリン耐性肺炎球菌(PRSP)
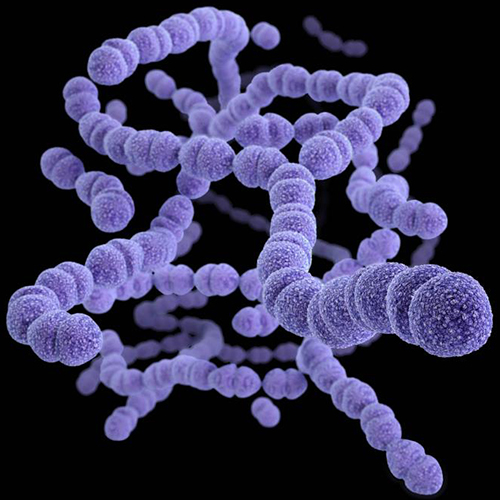
U.S. Centers for Disease Control and Prevention - Medical Illustrator.
肺炎球菌はこどもや成人の肺炎や中耳炎、さらには髄膜炎など重症感染症の原因にもなります。小児への結合型肺炎球菌ワクチン定期予防接種の普及により小児の重症肺炎球菌感染症の頻度は激減し、間接効果で成人の肺炎球菌感染症にも減少がみられています[2]。肺炎球菌が他の細菌と異なる点は、感染症により耐性か感受性かの判断が変わる点です。髄膜炎ですと「耐性」と判定する基準が厳しくなり、肺炎だと緩くなります。非髄膜炎の基準を用いると国内にはPRSPはほとんどいませんが、髄膜炎基準だと48%がPRSPです。抗菌薬使用量と耐性率がきれいに相関する細菌であり[3]、抗菌薬適正使用によりさらなる耐性率の減少が期待できます。ワクチンとAMR対策、双方からの対策が必要な細菌です。
基質拡張型ベータラクタマーゼ(ESBL)産生菌
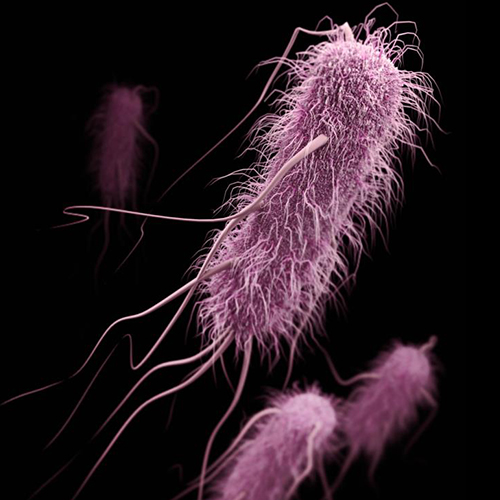
Illustrators: Alissa Eckert and Jennifer Oosthuizen.
ペニシリン、セフェム、カルバペネムなどのベータラクタム系抗菌薬を分解する酵素はベータラクタマーゼと呼ばれます。この酵素をもつ細菌はその種類によってさまざまな程度で抗菌薬を分解します。ESBLは細菌の名前ではなくべ-タラクタマーゼの一種であり、ペニシリンを分解するベータラクタマーゼである「ペニシリナーゼ」が変異し、より多くの抗菌薬(ペニシリン系、セフェム系)を分解できるようになったものです。ESBL産生菌もMRSA同様、以前は院内感染の原因菌として問題でしたが、現在は市中にも広く定着しつつあります。ESBL産生菌の治療にはカルバペネム系抗菌薬が用いられてきました。最近はピペラシリン・タゾバクタムやセファマイシン系抗菌薬によって治療可能であるというエビデンスが少しずつ集まってきています[4]。
抗菌薬投与がESBL獲得の危険因子であることは多くの研究で確認されており、抗菌薬適正使用が大切です。国によっては患者から分離される大腸菌のほとんどがESBL産生菌であり、そのような国では、広域抗菌薬の投与がさらにESBLを生み出すという悪循環に陥ります。また、鶏をはじめとした食肉から分離されることも多く、重要なリザーバーである可能性が指摘されています[5]。
AmpC産生菌
AmpCもESBL同様、ベータラクタマーゼの一種です。AmpCは多くの腸内細菌科細菌がもともと保持していますが、その量が少ない場合にはあまり大きな問題になりません。しかし、この酵素は抗菌薬曝露により誘導されることが知られており、誘導されて過剰に発現するとペニシリン系から第3世代セフェム系まで広範な薬剤耐性を獲得し、臨床上問題となります。EnterobacterやCitrobacterといった菌を治療中、「はじめは感受性があったのに、治療を開始したらあっという間に多剤耐性になった」ということはよくありますが、そのような場合はこのAmpCが原因であることが多いです。AmpCの発現遺伝子は染色体上の場合もプラスミド上の場合もあり、プラスミド上にある場合は、接合による菌同士の耐性遺伝子の受け渡しにより、クレブシエラなど本来AmpCを持たない細菌にも発現することがあります。
多剤耐性緑膿菌(MDRP)
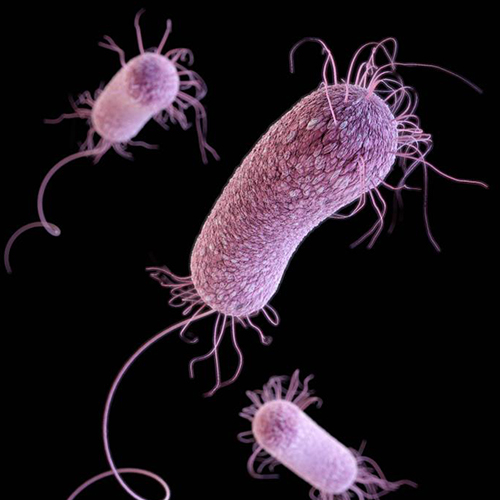
U.S. Centers for Disease Control and Prevention - Medical Illustrator.
緑膿菌は病原性そのものは弱いため、免疫が正常な人たちには感染症を起こしにくい細菌です。しかし、免疫不全、低栄養などの人たちを中心に、一度感染症を発症すると難治になります。本来、多剤耐性傾向の強い細菌であるため、抗緑膿菌作用のあるペニシリンやセファロスポリン系薬、モノバクタム系、カルバペネム系、フルオロキノロン系、アミノグリコシド系など限られた抗菌薬でしか治療ができません。さらに、耐性機構も多様で新たな薬剤耐性を獲得しやすく、上記の薬剤にも耐性となった緑膿菌が多く存在します。緑膿菌治療のキードラッグであるカルバペネム系、フルオロキノロン系、アミノグリコシド系のすべてに耐性となった緑膿菌をMDRPと呼びます。緑膿菌感染症の治療に使用できる薬剤がもともと少ないこともあり、緑膿菌の薬剤耐性は治療上の大きな問題となります。緑膿菌は環境を通して患者から患者へ広がっていくため、耐性緑膿菌に対しては治療だけでなく、他者へ伝搬させない感染対策も重要です。
カルバペネム耐性腸内細菌科細菌(CRE)
U.S. Centers for Disease Control and Prevention - Medical Illustrator.
2000年を超えたころより耐性菌治療の切り札であったカルバペネム系薬に耐性の腸内細菌科細菌(大腸菌やクレブシエラ、プロテウスなど、主に腸内でブドウ糖を発酵してエネルギーを得ている細菌)が発見され[6]、次々と世界に広がっていきました。中には現存するすべての抗菌薬に耐性である菌も存在するため、CREは「悪夢の耐性菌」と呼ばれ、現在世界で最も恐れられている耐性菌のひとつといえます。CREの耐性機構には種々ありますが、中でも「カルバペネマーゼ」というあらゆるベータラクタム系薬を分解してしまう酵素をもつ細菌を「カルバペネマーゼ産生腸内細菌科細菌(CPE)」と呼びます。インドで発見されたニューデリーメタロベータラクタマーゼ1(NDM-1)、アメリカでクレブシエラ・ニューモニエから発見されたKPCなどが有名ですが、日本ではIMPというタイプが最もよく検出されています。カルバペネマーゼを産生する遺伝子は一部の細菌を除いてプラスミド上に保持しているので、同種、異種を問わず細菌から細菌へ、まるでソーシャルネットワークのように拡散していきます。日本で過去に数件の病院内アウトブレイク事例があったこともあり、現在、感染症法に基づく届出により感染症例すべてを国に届け出することが義務化され、監視が強化されています。
関連文献
- Paulsen J, et al.: The Impact of Infectious Disease Specialist Consultation for Staphylococcus aureus Bloodstream Infections: A Systematic Review. Open Forum Infect Dis. 2016 Mar 1;3(2):ofw048. doi: 10.1093/ofid/ofw048. eCollection 2016 Mar.
- Whitney CG, et al.; Active Bacterial Core Surveillance of the Emerging Infections Program Network: Decline in invasive pneumococcal disease after the introduction of protein-polysaccharide conjugate vaccine. N Engl J Med. 2003 May 1;348(18):1737-46.
- World Health Organization(WHO): The evolving threat of antimicrobial resistance - Options for action. WHO. [cited 2017 May 25].
- Seo YB, et al.: Randomized controlled trial of piperacillin-tazobactam, cefepime and ertapenem for the treatment of urinary tract infection caused by extended-spectrum beta-lactamase-producing Escherichia coli. BMC Infect Dis. 2017 Jun 7;17(1):404. doi: 10.1186/s12879-017-2502-x.
- Overdevest I, et al.: Extended-spectrum β-lactamase genes of Escherichia coli in chicken meat and humans, The Netherlands. Emerg Infect Dis. 2011 Jul;17(7):1216-22. doi: 10.3201/eid1707.110209.
- Yigit H, et al.: Novel carbapenem-hydrolyzing beta-lactamase, KPC-1, from a carbapenem-resistant strain of Klebsiella pneumoniae. Antimicrob Agents Chemother. 2001 Apr;45(4):1151-61.


